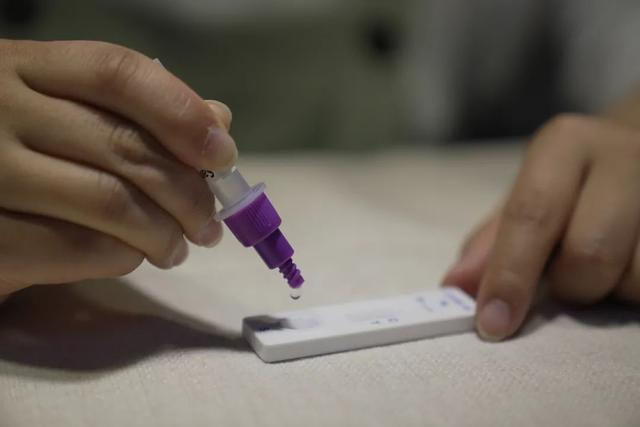
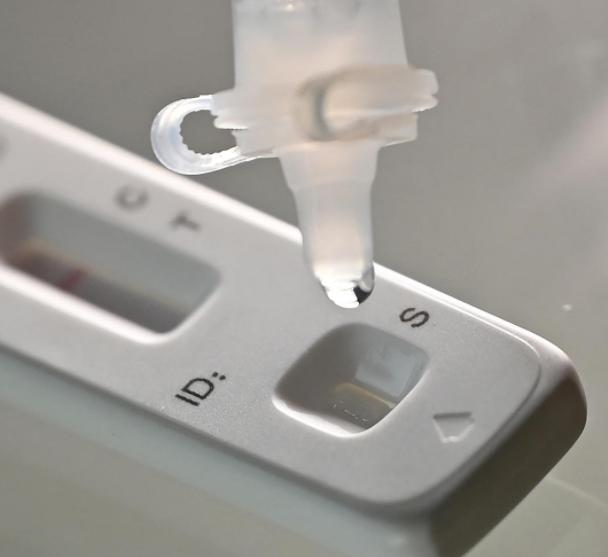
Pe 12 martieth 2022, celNMPA (SFDA) a emis o notificare prin care aprobă schimbarea cererii de autotestare a produselor cu antigen COVID-19 de către Nanjing Vazyme BiotechCo, Ltd, Tehnologia de bioinginerie Beijing JinwofuCo, Ltd, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd șiBeijing Savant Biotechnology Co.,ltd(Huaketai).Au fost lansate cinci produse de autotestare a antigenului COVID-19.
La 11 martie 2022, NHC a anunțat că, pentru a optimiza în continuare strategia de testare a noului coronavirus și pentru a servi nevoilor de prevenire și control al COVID-19, Echipa cuprinzătoare a Mecanismului comun de prevenire și control al Consiliului de Stat a decis să adauge testarea antigenului la testarea acidului nucleic și a făcut „Protocolul de aplicare pentru detectarea antigenului noului coronavirus (probă)”
Protocolul specifică populația aplicabilă pentru testarea antigenului:
În primul rând, cei care vizitează instituțiile medicale primare și au simptome precum căile respiratorii și febră în decurs de 5 zile de la apariția simptomelor;
În al doilea rând, personalul de observare a carantinei, inclusiv observarea carantinăi la domiciliu, contactul apropiat și contactul sub-aproape, observarea carantinării la intrare, personalul din zona de izolare și zona de control;
Al treilea este rezidenții comunității care au nevoie de autodetecția antigenului.
Sfaturi:Detecția antigenului este un supliment important al detectării acidului nucleic, dar rezultatele autodetecției antigenului nu pot fi folosite ca bază pentru diagnosticul infecției.
Ora postării: 22-mar-2022